法规事务咨询
法规事务咨询
从PMDA申请战略制定、事前咨询到申请分类选择,我们提供基于丰富经验的精准建议。以通俗易懂的方式解析日本法规要求,力争以最短时间获得批准。

Japan Regulatory Affairs
许多海外制造商认为日本PMDA的审批流程独特而复杂。实际上,只要采用合理的临床评价策略,并找到合适的本地合作伙伴,获批之路清晰可行。
了解更多服务内容
我们支持日本(PMDA)医疗器械法规申请的全流程——从战略咨询到完整的文件准备,助力海外制造商顺利进入日本市场。
法规事务咨询
从PMDA申请战略制定、事前咨询到申请分类选择,我们提供基于丰富经验的精准建议。以通俗易懂的方式解析日本法规要求,力争以最短时间获得批准。
临床评价报告
我们擅长通过临床评价获得PMDA批准——无需开展新的临床试验。从文献检索到临床评价计划及CER报告书的制作,提供基于科学评据的全流程支持。
Regulatory Approval Support
从设备分类确定到PMDA申请文件全套制作,全程支持药事批准取得。擅长临床评价方式的批准取得,并提供面向海外制造商的英文支持。
Business License Support
全程支持在日本制造、销售医疗器械所需的各类业许可,包括制造销售业许可、制造业登记及销售业备案等。
Specialty
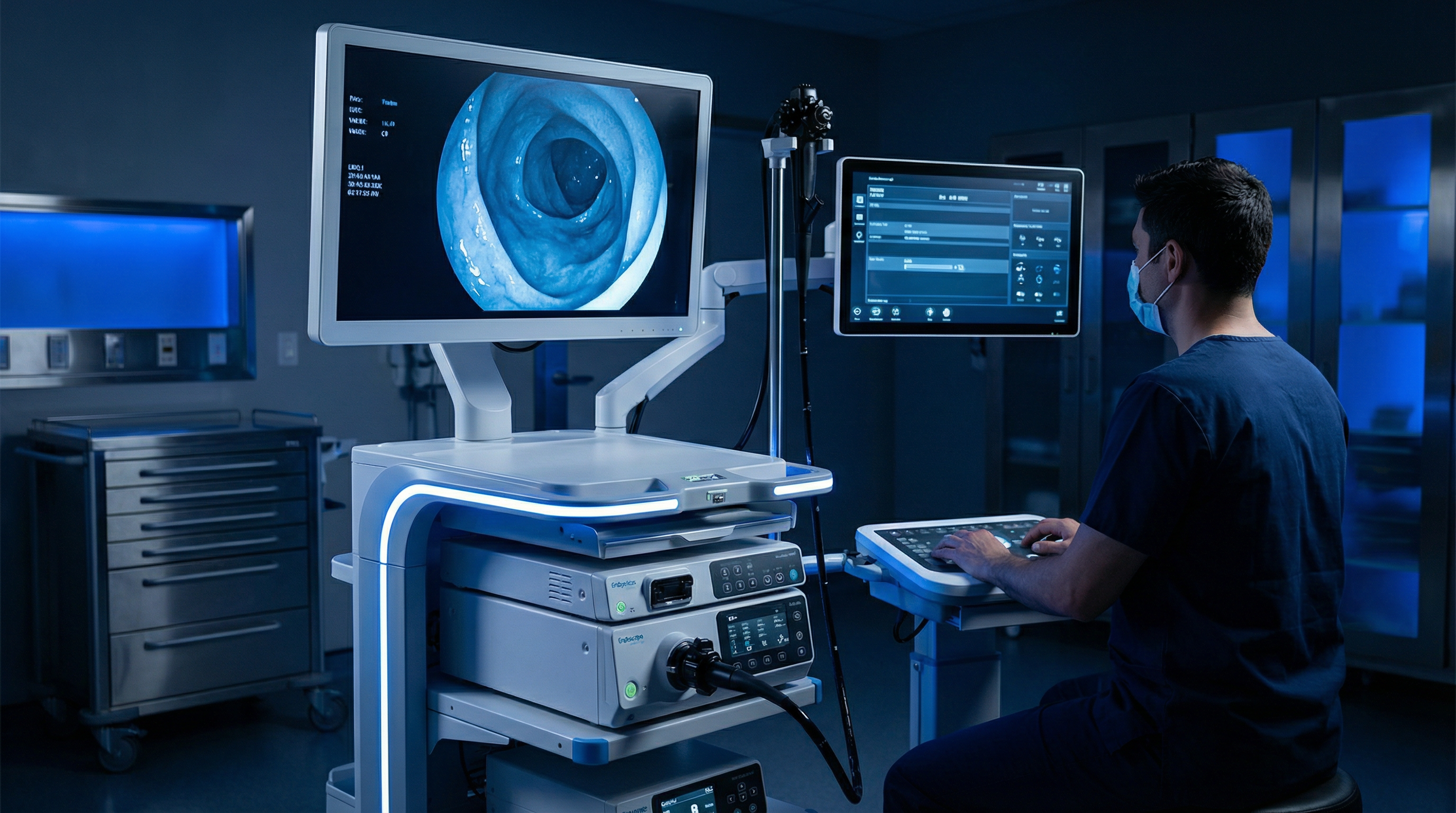
消化内镜 擅长领域
我们的优势
凭借深厚的专业知识与清晰的流程,帮助您的医疗器械高效进入日本市场。
消化内镜器械是我们的核心强项,涵盖内镜系统、处置器具及相关设备,对日本特有的法规要求有深入了解。当然,其他医疗器械领域的咨询也欢迎随时联系我们。
我们擅长利用现有临床文献和数据进行临床评价,无需开展新的临床试验即可获得PMDA批准,大幅降低成本与时间,同时确保顺利获批。
我们持续跟踪PMDA最新指南,迅速制作高质量的申请文件,将因文件缺陷导致退回的情况降至最低,实现顺畅的审查应对。
即使没有日本本地法规团队的制造商,也可放心委托我们。我们提供从项目进度管理到PMDA应对的全方位、一贯性支持。
代表致辞
日本是全球最大的医疗器械市场之一,也是最值得进入的市场之一。从外部看,PMDA的法规框架似乎复杂,但实际上,只要掌握正确的专业知识和策略,获批之路清晰可循。
MK咨询株式会社作为医疗器械制造商——无论国内还是海外——进入日本市场的可靠本地合作伙伴而成立。我们在消化内镜领域积累的丰富经验,以及通过临床评价获得批准的专业知识,使我们能够高效引导客户完成PMDA审批流程。
尤其是我们的临床评价方案——无需开展新的临床试验即可获得批准——在大幅降低开发成本与时间的同时,实现了基于科学证据的批准获取。我们始终紧跟最新法规动态,为每位客户量身定制最优策略。
进入日本市场是完全可以实现的目标。让我们助您达成。欢迎随时与我们联系咨询。
代表取締役
觉野 讲平
MK咨询株式会社 代表取締役

公司概况
提供日本(PMDA)医疗器械法规申请相关咨询及申请文件代理制作服务。消化内镜领域是我们的强项,其他医疗器械领域也欢迎随时咨询。擅长通过临床评价获得批准。
〒231-0005
日本神奈川县横滨市中区本町4丁目41番地
5020001152593
FAQ
整理了海外医疗器械制造商就日本市场进入及PMDA申请的常见问题。
联系我们
如有关于日本法规申请(PMDA)、临床评价或文件代理制作的咨询,欢迎随时联系我们。通常将在2至3个工作日内回复。