약사 신청 컨설팅
약사 신청 컨설팅
PMDA 신청 전략 수립, 사전 상담, 기기 분류 결정까지 풍부한 경험에 기반한 정확한 조언을 제공합니다. 일본의 복잡한 규제 요건을 명확하게 설명하고 최단 기간 내 승인 취득을 목표로 합니다.

Japan Regulatory Affairs
많은 해외 제조사들이 일본 PMDA 승인 절차가 복잡하다고 생각합니다. 하지만 체계적인 임상평가 전략과 올바른 현지 파트너가 있다면, 승인의 길은 명확하고 관리 가능합니다.
자세히 보기서비스
일본(PMDA) 의료기기 규제 신청의 전 과정을 지원합니다. 전략 컨설팅부터 완전한 서류 준비까지, 일본 시장 진출을 원하는 해외 제조사를 위해 최선을 다합니다.
약사 신청 컨설팅
PMDA 신청 전략 수립, 사전 상담, 기기 분류 결정까지 풍부한 경험에 기반한 정확한 조언을 제공합니다. 일본의 복잡한 규제 요건을 명확하게 설명하고 최단 기간 내 승인 취득을 목표로 합니다.
신청서류 작성 대행
승인 신청서 및 첨부 자료(개요서, 설계 검증·타당성 확인 자료 등)의 작성을 대행합니다. PMDA가 요구하는 품질과 형식에 맞게 정확하고 신속하게 작성합니다.
임상평가 보고서
임상평가 기반 PMDA 승인 취득을 전문으로 합니다. 새로운 임상시험 없이 기존 임상 문헌과 데이터를 활용합니다. 문헌 조사부터 임상평가 계획 및 CER 보고서 작성까지 과학적 근거에 기반한 전 과정을 지원합니다.
Regulatory Approval Support
기기 분류 확정부터 PMDA 신청 서류 일식 작성까지 약사 승인 취득을 일관 지원합니다. 임상평가 방식의 승인 취득을 전문으로 하며, 해외 제조사를 위한 영어 대응도 가능합니다.
Business License Support
일본에서 의료기기를 제조·판매하기 위해 필요한 제조판매업 허가·제조업 등록·판매업 신고 등 모든 업허가 취득을 일관 지원합니다.
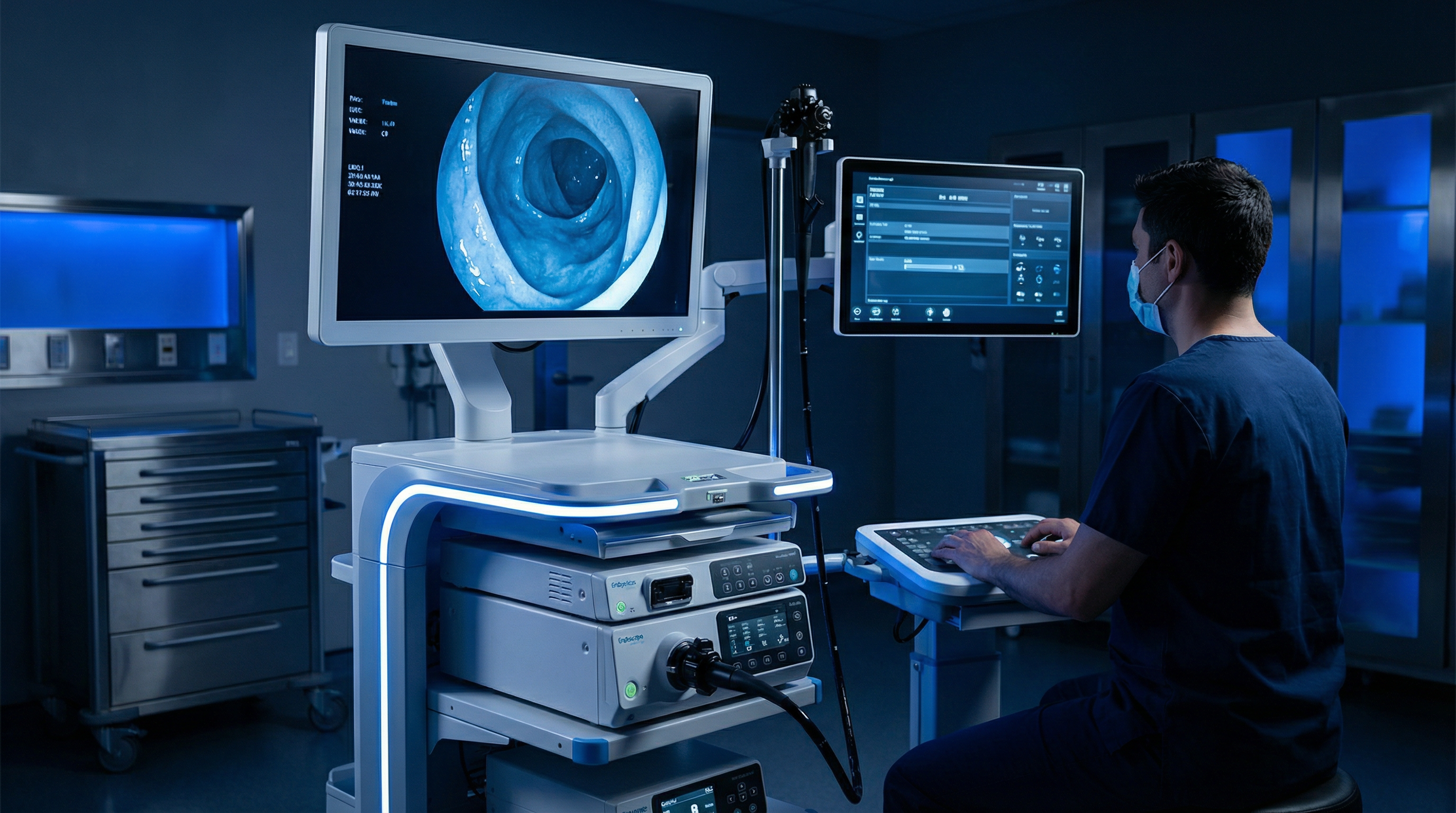
Specialty
소화기 내시경 특기 분야
저희의 강점
깊은 전문성과 명확한 프로세스로 귀사의 의료기기가 일본 시장에 효율적으로 진출할 수 있도록 지원합니다.
소화기 내시경 기기가 핵심 특기 분야로, 내시경 시스템·처치 기구·관련 기기에서 일본 특유의 규제 요건을 완벽히 이해하고 있습니다. 물론 다른 의료기기 분야에 대한 문의도 언제든지 환영합니다.
기존 임상 문헌과 데이터를 활용한 임상평가를 통해 PMDA 승인을 취득하는 것을 전문으로 합니다. 새로운 임상시험 없이 비용과 기간을 크게 절감하면서 확실한 승인 취득을 실현합니다.
PMDA의 최신 가이던스를 항상 파악하고 고품질의 신청 서류를 신속하게 작성합니다. 서류 미비로 인한 반려를 최소화하고 원활한 심사 대응을 실현합니다.
일본 현지 규제 팀이 없는 제조사도 안심하고 의뢰하실 수 있습니다. 프로젝트 진행 관리부터 PMDA 대응까지 일관되게 지원합니다.
대표 인사말
일본은 세계 최대 의료기기 시장 중 하나이며, 진출할 가치가 충분한 시장입니다. 외부에서 보면 PMDA의 규제 체계가 복잡해 보일 수 있지만, 올바른 전문 지식과 전략이 있다면 승인의 길은 명확하고 충분히 헤쳐나갈 수 있습니다.
MK컨설팅 주식회사는 국내외 의료기기 제조사가 일본 시장 승인을 취득하는 데 있어 신뢰할 수 있는 현지 파트너로서 설립되었습니다. 소화기 내시경 분야의 풍부한 경험과 임상평가 기반 승인 취득의 전문 지식으로 PMDA 심사 과정을 효율적으로 안내해 드립니다.
특히 새로운 임상시험 없이 승인을 취득하는 임상평가 방식은 개발 비용과 기간을 크게 절감하면서도 과학적 근거에 기반한 결과를 제공합니다. 저희는 최신 규제 동향을 항상 파악하며 각 고객의 상황에 맞는 최적의 전략을 제안합니다.
일본 시장 진출은 충분히 달성 가능한 목표입니다. 저희가 함께하겠습니다. 언제든지 편하게 문의해 주세요.
대표이사
카쿠노 코헤이
MK컨설팅 주식회사 대표이사

회사 개요
일본(PMDA) 의료기기 약사 신청 관련 컨설팅 및 신청서류 작성 대행 서비스. 소화기 내시경 분야가 특기이지만, 다른 의료기기 분야도 언제든지 상담해 드립니다. 임상평가 기반 승인 취득 특기.
〒231-0005
일본 가나가와현 요코하마시 나카구 혼초 4-41
5020001152593
FAQ
해외 의료기기 제조사들이 일본 시장 진입 및 PMDA 신청에 대해 자주 묻는 질문을 정리했습니다.
문의하기
일본 약사 신청(PMDA), 임상평가, 서류 작성 대행에 관한 문의는 언제든지 환영합니다. 통상 2~3 영업일 이내에 답변 드립니다.